Introducción
La presencia de micotoxinas en los piensos representa un riesgo significativo para la salud animal (Muñoz-Solano et al., 2024). Su consumo puede desencadenar síntomas clínicos que están relacionados con la alteración en la expresión de ciertos genes, lo que afecta a procesos biológicos clave.
El estudio de la modificación de la expresión génica es una herramienta fundamental para evaluar el impacto de las micotoxinas y diseñar estrategias efectivas para minimizar sus efectos adversos. En este contexto, los fitogénicos, gracias a sus componentes activos, han demostrado su capacidad para modular la expresión de genes específicos en especies productivas. En consecuencia, interaccionan antagónicamente con las micotoxinas, reduciendo así los efectos clínicos causados y contribuyendo a una mejora del estado de salud de los animales.
La modificación de la expresión genética que producen los extractos fitogénicos se enfoca en procesos biológicos clave, disminuyendo el estrés oxidativo, mejorando la salud intestinal y equilibrando la microbiota, entre otros beneficios. Estos factores están estrechamente relacionados con la mitigación de los efectos perjudiciales de las micotoxinas en nutrición animal.
Interacciones entre micotoxinas y genes
Según las interacciones que se han detectado sobre los genes relacionados con las principales micotoxinas -Aflatoxina B1 (AFB1), Fumonisina B1 (FB1), Deoxinivalenol (DON), Zearalenona (ZEA), Ocratoxina A (OTA), Toxina T-2 (T-2)- registradas en la base de datos PubChem (NCBI), (PubChem, https://pubchem.ncbi.nlm.nih.gov/), se puede observar que las micotoxinas citadas pueden interaccionar con los mismos genes, estableciéndose efectos aditivos y sinérgicos entre ellas.
En el Gráfico 1 se ilustra el número de genes cuya expresión se ve alterada con la presencia de las micotoxinas, y la relación que existe entre los genes de cada micotoxina. Se puede observar que existen 75 genes comunes los cuales son modificados por la presencia de todas las micotoxinas principales citadas, y que existe una alta correlación entre genes modulados por AFB1, DON y ZEA.
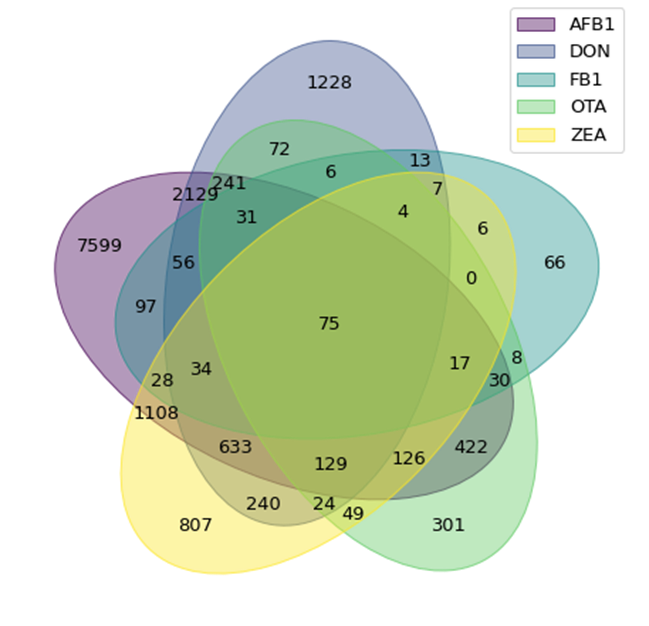
Gráfico 1. Diagrama de Venn de las interacciones de genes producidas por las principales micotoxinas.
Entre el número total de genes involucrados con la toxicidad de las micotoxinas, estos se pueden clasificar según la función en la cual el gen está interviniendo. De esta manera, se podrían destacar cinco grupos principales de genes los cuales están relacionados según su funcionalidad biológica:
- Inflamación y respuesta inmune
- Apoptosis
- Barrera epitelial
- Metabolismo y respuesta antioxidante
- Metabolismo hormonal
Como se puede observar en la Tabla 1 todas las micotoxinas tienen efectos relacionados en la inflamación, la respuesta inmune y la apoptosis. Siendo únicamente la Zearealenona la que presenta interacciones con el metabolismo hormonal.
| Micotoxina | Inflamación y respuesta inmune | Apoptosis | Barrera epitelial | Metabolismo y respuesta antioxidante | Metabolismo hormonal |
|---|---|---|---|---|---|
| Aflatoxina B1 (AFB1) | X | X | X | ||
| Deoxinivalenol (DON) | X | X | X | ||
| Zearealenona (ZEA) | X | X | X | ||
| Ocratoxina A (OTA) | X | X | X | X | |
| Toxina T-2 (T-2) | X | X | X | X | |
| Fumonisina B1 (FB1) | X | X | X | X |
Tabla 1. Resumen de la clasificación de las principales micotoxinas por las familias de genes que modifican según su función.
Interacciones genéticas de la Aflatoxina B1
Principales síntomas clínicos de la intoxicación por AFB1:
- Falta de apetito y pérdida de peso (Fouad et al., 2019)
- Ictericia por daño hepático (Popescu et al., 2022; Mallmann et al., 2007).
- Hemorragias internas y problemas de coagulación (Ochieng., et al. (2016).
- Diarrea y vómitos (Hernández-Martínez et al., 2023)
- Inmunosupresión (Saleemi et al., 2020; Sohrabi et al., 2023)
- Problemas reproductivos (Fouad et al., 2019)
- Retraso en el crecimiento (Ochieng et al., 2021)
Principales interacciones con genes:
Metabolismo de xenobióticos y biotransformación: CYP1A1, CYP1A2, CYP2A13, CYP3A4, CYP3A37, CYP19A1, EPHX1, GSTA3, GSTA5, ALDH1A1, AKR7A3, GNMT. |
Regulación del ciclo celular y apoptosis: TP53, CDKN1A, MDM2, BAX, BCL2, CASP3, CASP8, FAS, WWOX. |
Respuesta al daño del ADN y estrés celular: H2AX, MGMT, PRKN. |
Inflamación y respuesta inmune: IL6, PTGS2, GDF15. |
Respuesta antioxidante y protección celular: CAT, NFE2L2. |
Señalización celular y regulación génica: MAPK1, ITPR3, BTG2, ATF3, VDR. |
Tabla 2. Principales interacciones con genes producidas por la Aflatoxina B1.
Interacciones genéticas del Deoxinivalenol
Principales síntomas clínicos asociados a la intoxicación por DON:
- Rechazo del alimento y pérdida de peso (Ogunade et al., 2018; Mallmann et al., 2007)
- Vómitos y diarrea (Ochieng et al., 2021)
- Inmunosupresión (Hasuda et al., 2022)
- Reducción en la producción de leche, carne o huevos (Ruhnau et al., 2020; Jia et al., 2023)
- Alteraciones en la integridad del tracto gastrointestinal: enteritis necrótica (Ruhnau et al., 2020; Jia et al., 2023)
Principales interacciones con genes:
Inflamación y respuesta inmune: IL6, TNF, IL1B, IL1A, IL10, IL18, CXCL8, IFNG. |
Apoptosis y supervivencia celular: CASP3, BCL2. |
Función de la barrera epitelial: CLDN1, TJP1, OCLN. |
Señalización celular y respuesta al estrés: MAPK1, MAPK3, MAPK8, MAPK9, ATF3, JUN, AHR. |
Regulación de mediadores proinflamatorios: PTGS2. |
Tabla 3. Principales interacciones con genes producidas por el Deoxinivalenol.
Interacciones genéticas de la Zearealenona
Principales síntomas clínicos de la intoxicación por ZEA:
- Inflamación y enrojecimiento de la vulva (vulvovaginitis) (Hartinger et al., 2022)
- Prolapso vaginal en hembras jóvenes (Dinev et al., 2021)
- Abortos o partos prematuros (Ogunade et al., 2018; Nikolov et al., 2023)
- Disminución de la fertilidad y problemas en la ovulación (Liu et al., 2020)
Principales interacciones con genes:
Inflamación y respuesta inmune: IL1B, TNF, IL6, IL18, IL1A, CCL2, CXCL8, NLRP3, RELA. |
Apoptosis y supervivencia celular: CASP3, CASP1, CASP9, BAX, BCL2, CYCS, PYCARD. |
Metabolismo y detoxificación: CYP3A4, ABCC1, ABCC2, ABCG2, GPT, HMOX1, NFE2L2. |
Señalización celular y regulación del ciclo celular: MAPK1, MAPK3, TP53, PPARG. |
Hormonas y receptores nucleares: ESR1, ESR2, AR, PGR, CGA. |
Tabla 4. Principales interacciones con genes producidas por la Zearalenona.
Interacciones genéticas de la Ocratoxina A
Principales síntomas clínicos de la intoxicación por OTA A:
- Daño renal (nefropatía) (Tassis et al., 2024; Ceci et al., 2007; Mallmann et al., 2007)
- Daño hepático (Awais et al., 2022)
- Pérdida de peso y retraso en el crecimiento (Vasiljević et al., 2021)
- Inmunosupresión (mayor riesgo de infecciones)
- Problemas reproductivos en hembras y machos (Malir et al., 2014)
Principales interacciones con genes:
Inflamación y respuesta inmune: IL1B, TNF, IL6, IL18, IL1A, CXCL8, CCL2. |
Apoptosis y muerte celular programada: CASP3, CASP9, BAX, BCL2, CYCS, TP53. |
Necroptosis y piroptosis (muerte celular inflamatoria): GSDMD, MLKL, RIPK1, RIPK3. |
Metabolismo y respuesta antioxidante: NFE2L2, NR1H2, NR1H3. |
Integridad de la barrera epitelial: OCLN. |
Tabla 5. Principales interacciones con genes producidas por la Ocratoxina A.
Interacciones genéticas de la Toxina T-2
Principales síntomas clínicos de la intoxicación por Toxina T-2:
- Vómitos y diarrea
- Pérdida de apetito (anorexia) y pérdida de peso
- Letargo y debilidad. (Vörösházi et al., 2024)
- Hemorragias internas en el tracto gastrointestinal, hígado, y riñones
- Daño en las mucosas y lesiones dermatológicas (inflamación en el tracto gastrointestinal y necrosis) (Wojtacha et al., 2021, Gómez et al., 2024, Sandu, 2023; Gjevre, 2013)
- Convulsiones y temblores en casos graves (efectos neurotóxicos) (Ogunade et al., 2018; Kemboi et al., 2020)
- Alteraciones en la reproducción (problemas de fertilidad y parto prematuro en animales
Principales interacciones con genes:
Inflamación y respuesta inmune: IL1B, IL6, TNF. |
Apoptosis y muerte celular programada: CASP3, CASP8, CASP9, BAX. |
Respuesta al estrés celular y daño del ADN: DDIT3, EIF2S1, HSPA5, CDKN1A. |
Respuesta antioxidante y protección celular: NFE2L2, CAT. |
Degradación de la matriz extracelular y remodelación tisular: MMP13, ACAN. |
Tabla 6. Principales interacciones con genes producidas por la Toxina T-2.
Interacciones genéticas de la Fumonisina B1
Principales síntomas clínicos de la intoxicación por FB1:
- Insuficiencia hepática: ictericia (coloración amarillenta de la piel y mucosas) y disfunción hepática (Hartinger et al., 2022)
- Daño renal: poliuria (micción excesiva), polidipsia (excesiva sed) y deshidratación (Kulcsár et al., 2023)
- Síndrome del edema pulmonar (Haschek., et al. 2001)
- Pérdida de peso y disminución del apetito.
Síntomas crónicos
- Enfermedades hepáticas crónicas (cirrosis, fibrosis) y cáncer hepático (Anumudu et al., 2024)
- Trastornos reproductivos: reducción en la fertilidad y en la producción de leche (Alhelaisi et al., 2023)
- Problemas en la crecimiento y desarrollo de los animales
Principales interacciones con genes:
Inflamación y respuesta inmune: IL1B, TNF, IL6, IL18, IL1A, CXCL8, CCL2. |
Apoptosis y muerte celular programada: CASP3, CASP9, BAX, BCL2, CYCS, TP53. |
Necroptosis y piroptosis (muerte celular inflamatoria): GSDMD, MLKL, RIPK1, RIPK3. |
Metabolismo y respuesta antioxidante: NFE2L2, NR1H2, NR1H3. |
Integridad de la barrera epitelial: OCLN. |
Tabla 7. Principales interacciones con genes producidas por la Fumonisina B1.
Estrategias para afrontar el desafío de las micotoxinas
Para mitigar los síntomas clínicos inducidos las micotoxinas, las soluciones anti-micotoxinas disponibles en el mercado implementan diversas estrategias destinadas a minimizar sus efectos en la productividad y salud animal. Entre estas estrategias, destaca el mecanismo de adsorción mediante el uso de adsorbentes minerales y/o levaduras, el cual puede combinarse con el empleo de aditivos fitogénicos, potenciando la eficacia del tratamiento, lo que se traduce en una mejora significativa en la salud y la productividad animal. Este enfoque se fundamenta en las interacciones genéticas inducidas por los compuestos activos presentes en los aditivos fitogénicos que incluyen las formulaciones de los agentes anti-micotoxinas.
Las combinaciones de fitogénicas contienen una selección de extractos cuyas sustancias activas exhiben un efecto sinérgico en la mitigación de los efectos negativos de las micotoxinas. La acción combinada de estos compuestos mejora la eficacia de cada extracto, lo que permite una reducción más efectiva de la toxicidad y el impacto de las micotoxinas. Este efecto sinérgico se logra mediante mecanismos complementarios que optimizan la modulación de las respuestas biológicas asociadas, favoreciendo así la salud y el rendimiento productivo de los animales.
Interacciones entre combinaciones de fitogénicos para contrarrestar el efecto de las micotoxinas
El análisis de las interacciones genéticas, representado en el Gráfico 2, evidencia la relación entre los genes afectados por la presencia de micotoxinas y aquellos cuya modulación puede ser regulada a través de las combinaciones de compuestos bioactivos presentes en los extractos fitogénicos.
Además, los diagramas de Venn muestran los genes comunes cuya expresión puede ser modulada mediante el uso de estos aditivos. Como se observa, la aplicación conjunta de las diferentes combinaciones de extractos fitogénicos pueden generar efectos potenciadores (cuando ambas combinaciones de extractos modulan los mismos genes afectados por las micotoxinas) y complementarios (cuando cada combinación de extractos modula diferentes genes involucrados en la respuesta a las micotoxinas).
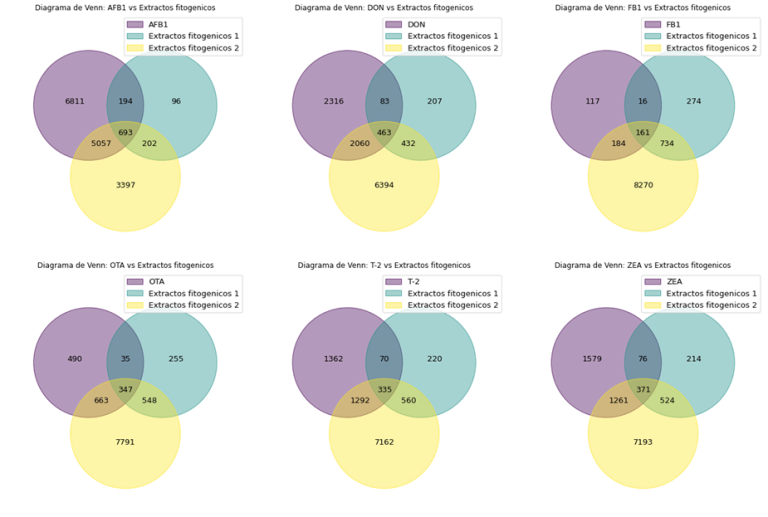
Gráfico 2. Diagramas de Venn de las interacciones de genes inducidas por las diferentes micotoxinas en comparación con las soluciones fitogenicas anti-micotoxinas.
Si observamos la combinación de extractos fitogénicos 1, que es una combinación de curcuma longa (curcumina) y Silybum marianum (cardo mariano); y la combinación de extractos fitogénicos 2, que contiene extractos de uva y oliva; se puede observar que presentan una respuesta destacada frente a genes de inflamación, respuesta inmune, apoptosis, respuesta antioxidante y muerte celular. De esta manera, no solo es posible contrarrestar los síntomas clínicos inducidos por micotoxinas, sino también aquellos provocados por otras situaciones, como distintas condiciones de estrés que puedan afectar a los animales.
Estos hallazgos refuerzan la importancia de los fitogénicos y sus combinaciones como una estrategia efectiva para mitigar los efectos de las micotoxinas a nivel molecular, ofreciendo un enfoque innovador y natural para mejorar la salud y el rendimiento de los animales.
A continuación, se describen las principales interacciones con genes de los fitogénicos citados anteriormente.
Interacciones genéticas del extracto de cúrcuma longa
Bioactivos principales: El extracto de cúrcuma longa presenta diferentes curcominoides entre los que destaca la curcumina.
Inflamación y respuesta inmune: TNF, IL1B, IL6, IL10, IL18, CXCL8, TLR4, PTGS2, IFNG. |
Apoptosis y muerte celular: CASP1, CASP3, CASP7, CASP8, CASP9, BAX, BCL2, XIAP, PARP1. |
Señalización celular: MAPK1, AKT1, STAT3, EP300, RELA, NFKB1, MTOR. |
Metabolismo y antioxidantes: NFE2L2, HMOX1, SOD1, GSTP1, GSR. |
Ciclo celular: TP53, CDKN1A, CCND1. |
Tabla 8. Principales interacciones con genes producidas por los bioactivos del extracto de cúrcuma.
Interacciones genéticas del extracto de cardo mariano
Bioactivos principales: el extracto de cardo mariano es rico en diferentes compuestos flavonoides como la silibina, isosilibina, silicristina e isosilicristina, silidianina y taxifolina.
Inflamación y respuesta inmune: TNF, IL1B, IL6, IL10, IFNG, TGFB1, CXCL8, S100B, GDF15. |
Apoptosis y muerte celular: CASP1, CASP3, CASP9, BAX, BCL2, BID, PARP1. |
Respuesta antioxidante y metabolismo de xenobióticos: NFE2L2, HMOX1, CAT, SOD1, GSR, NQO1, KEAP1, GCLM, GSTA4, CYP2E1. |
Señalización celular y transducción de señales: MAPK1, MAPK3, MAPK8, MAPK9, RELA, PPARG, PPARA, SREBF1. |
Regulación del ciclo celular: TP53, CDKN1A, CDKN1B, CCND1, CDK2, CDK4, CHEK2, PCNA. |
Metabolismo y funciones fisiológicas: INS1, GPT, ACACA. |
Remodelación tisular, angiogénesis y matriz extracelular: MMP2, MMP9, COL1A1, VEGFA, ACTA2. |
Tabla 9. Principales interacciones con genes producidas por componentes activos del extracto de cardo mariano.
Interacciones genéticas del extracto de oliva
Bioactivos principales: el extracto de oliva contiene potentes antioxidantes, tales como el hidroxitirosol.
Inflamación y respuesta inmune: TNF, IL6, IL5, CCL5, PTGS2, VCAM1, ICAM1, SELE, STAT2, CSF1R, RELA. |
Apoptosis y muerte celular: CASP3, BAX, BCL2, DDIT3, FASTK, GADD45A. |
Respuesta antioxidante y metabolismo energético: CAT, SOD2, GPX2, GSR, NFE2L1, XDH, UCP2, TFAM. |
Señalización celular y proliferación: MAPK1, MAPK3, MAPKAPK2, AKT1, PPARA, PPARG, RPA3, EGR1, JUN, CEBPA, CDC25A. |
Metabolismo y función mitocondrial: ND1, ND2, COX1, COX4, CPT1B, FABP4, ADIPOQ, CYCB. |
Remodelación tisular, angiogénesis y matriz extracelular: MMP9, VEGFA, FGF1, COL1A1. |
Tabla 10. Principales interacciones con genes producidas por componentes activos del extracto de oliva.
Interacciones genéticas del extracto de uva
Bioactivos principales: El extracto de uva, proveniente de piel y semilla, contiene una amplia variedad de compuestos polifenólicos, entre los cuales destacan las antocianinas, flavonoides y flavoles, que poseen propiedades antioxidantes y antiinflamatorias, como las catequinas. También se encuentran los compuestos no flavonoides, especialmente el resveratrol y los ácidos fenólicos, los cuales contribuyen a mejorar la salud cardiovascular y a la prevención del cáncer.
Inflamación y respuesta inmune: TNF, IL1B, IL6, IL10, NLRP3, RELA, IFNG, IL2, IL4, IL21R, PTGS2, CXCL2, CXCL8, CCL2, CCL3, CCL4, CCR1, CCR2, CCR4, CD4, CD68, HAVCR2, F3. |
Apoptosis y muerte celular: CASP1, CASP3, BAX, BCL2, PYCARD, PARP1, CASP8, MCL1, TP53. |
Respuesta antioxidante y metabolismo de xenobióticos: NFE2L2, HMOX1, CAT, NOS2, KEAP1, GPX2, GSTA5, GSTM1, CYP1A1, CYP1A2, CYP1B1, CYP2B2, NQO1, GSR, GSTM2, GSTP1, MGST1, XDH, NOS3, PRDX5, ALOX5, ALOX15, CYP2E1. |
Señalización celular y transducción de señales: AKT1, MAPK1, MAPK3, MAPK14, GSK3B, DUSP1, PIK3CA, PIK3R1, JAK1, JAK2, TYK2, EGFR, PTK2. |
Metabolismo de lípidos y colesterol: SREBF2, CYP51A1, DHCR7, FDFT1, FDPS, HMGCR, HMGCS1, INSIG1, SQLE, SC5D, ACAT2, PPID, PPARG, LDLR. |
Angiogénesis y factores de crecimiento: PDGFA, PDGFB, VEGFA, EGF, PDGFBB, FLT4, EDN1, PDCD10. |
Tabla 11. Principales interacciones con genes producidas por componentes activos del extracto de uva.
Conclusiones
La evaluación de las interacciones genéticas inducidas por micotoxinas y por los compuestos activos presentes en extractos fitogénicos ha demostrado que estos últimos pueden modular dichas interacciones de manera beneficiosa. En consecuencia, la utilización de productos anti-micotoxinas que combinan fitogénicos seleccionados, como estrategia complementaria a la adsorción, potencia la eficacia en la mitigación de los efectos perjudiciales de la exposición a micotoxinas, de forma natural e innovadora, mejorando tanto la salud como el rendimiento de las explotaciones.


