La barrera intestinal: primera línea de defensa biológica
El tracto gastrointestinal no representa únicamente el eje central para la digestión y absorción de nutrientes, sino que constituye la primera barrera fisiológica contra los contaminantes presentes en el alimento (Assunçao et al., 2020; Alassane-Kpembi et al., 2019). En la actualidad, el desafío que plantean las micotoxinas es global y persistente, estimándose que estos metabolitos secundarios de origen fúngico contaminan entre el 60% y el 80% de los cultivos a nivel mundial (Gasperini et al., 2025; Guerre, 2020).
Una vez ingeridas, estas toxinas llegan al lumen intestinal, donde ejercen un impacto directo sobre la integridad de la mucosa. Este proceso compromete de manera simultánea la viabilidad de las células epiteliales, la funcionalidad de la capa de moco y la estabilidad del ecosistema microbiano, rompiendo la homeostasis necesaria para una producción animal eficiente y saludable (Gasperini et al., 2025; Celi et al., 2017).
Permeabilidad intestinal: barrera selectiva
La integridad estructural y funcional de la barrera intestinal depende intrínsecamente de las uniones estrechas, complejos proteicos de alta especialización que mantienen unidas las membranas laterales de los enterocitos (Figura 1). Estos complejos actúan como un sellado dinámico entre células adyacentes, estableciendo una barrera protectora continua cuya misión fundamental es la regulación selectiva del flujo de moléculas desde del lumen hacia el torrente sanguíneo (Gasperini et al., 2025; Zhai et al., 2021).
La funcionalidad de las uniones estrechas se fundamenta en una interacción precisa entre diversos grupos proteicos que dictan la estabilidad de la barrera. En este entramado, las proteínas transmembrana, tales como las claudinas (1, 3 y 4), la ocludina, la tricelulina y las moléculas de adhesión de la unión (JAMs), se proyectan hacia el espacio intercelular para consolidar un sello físico robusto. No obstante, la eficacia de este complejo depende directamente de las proteínas de andamiaje citoplasmático, entre las que destaca la ZO-1, vinculando las proteínas transmembrana con el citoesqueleto de actina para garantizar la estabilidad mecánica y la regulación dinámica del poro paracelular (Gao et al., 2018; Huang et al., 2022; Zhai et al., 2021).
Bajo condiciones fisiológicas óptimas, las uniones estrechas actúan como un filtro selectivo que favorece la absorción de nutrientes y electrolitos mientras que restringe el paso de antígenos y patógenos al torrente sanguíneo (Gasperini et al., 2025; Zhai et al., 2021). En el ámbito técnico, la integridad del epitelio se monitoriza mediante la resistencia eléctrica transepitelial (TEER), de manera que una reducción de este parámetro es un indicador inequívoco de que la barrera ha sido comprometida (Gao et al., 2018; Huang et al., 2022; Zhai et al., 2021).
Micotoxinas: el colapso de las uniones estrechas
La permeabilidad del epitelio puede verse afectada por múltiples causas, entre las que se encuentran las micotoxinas. Dentro de estos metabolitos químicamente diversos, las vías de toxicidad por las que alteran la integridad de esta estructura son diferentes. Por un lado, algunas de las micotoxinas más prevalentes, como el deoxinivalenol (DON) y la ocratoxina A (OTA) destacan por su capacidad para reducir drásticamente la TEER y, por tanto, aumentar la permeabilidad intestinal (Gao et al., 2018; Antonissen et al., 2014). Mientras que el DON ejerce su toxicidad mediante la inhibición de la síntesis de proteínas a nivel ribosomal, afectando específicamente a la expresión de la claudina-4, la OTA interviene alterando la estructura fundamental de la ocludina (Gasperini et al., 2025; Pierron et al., 2016).
Por otro lado, la zearalenona (ZEA) induce un daño mecánico diferencial a través de la activación de la vía de señalización RhoA/ROCK. Este mecanismo desencadena una remodelación del citoesqueleto de actina que altera la permeabilidad del epitelio de forma severa (Huang et al., 2022). De manera complementaria, las toxinas T-2 y HT-2 actúan sobre la expresión genética de la claudina-1, la ocludina y la ZO-1, precipitando una pérdida de adherencia celular que actúa como puerta de entrada para diversos patógenos entéricos (He et al., 2023).
De igual forma, e incluso en concentraciones que podrían considerarse bajas, las aflatoxinas (AFB1 y AFM1) han demostrado alterar la distribución de las uniones estrechas (Gao et al., 2018; Gasperini et al., 2025). Finalmente, las fumonisinas presentan un mecanismo de acción único: al inhibir la ceramida sintasa, alteran la composición de los esfingolípidos de membrana, comprometiendo la formación y el mantenimiento de las uniones estrechas desde la propia estructura lipídica de la célula (Bergen et al., 2025; Gasperini et al., 2025).
| Micotoxina | Mecanismo de acción principal | Proteínas/vías afectadas | Consecuencia funcional |
|---|---|---|---|
| Deoxinivalenol (DON) | Inhibición de la síntesis de proteínas a nivel ribosomal | Expresión de la claudina-4 | Reducción drástica de la TEER e incremento del flujo paracelular |
| Ocratoxina A (OTA) | Alteración de la estructura proteica fundamental | Estructura de la ocludina | Reducción drástica de la TEER e incremento del flujo paracelular |
| Zearalenona (ZEA) | Activación de una vía de señalización celular | Vía de señalización RhoA/ROCK, que remodela el citoesqueleto de actina | Compromiso severo de la permeabilidad epitelial |
| Toxinas T-2 y HT-2 | Alteración de la expresión genética | Expresión de claudina-1, ocludina y ZO-1 | Pérdida de adherencia celular, creando una puerta de entrada para patógenos entéricos |
| Aflatoxinas (AFB1, AFM1) | Modificación de la localización de proteínas | Distribución de las uniones estrechas | Alteración de la barrera incluso a bajas concentraciones |
| Fumonisinas | Inhibición de la síntesis de lípidos de membrana | Ceramida sintasa, afectando la composición de esfingolípidos | Compromiso de la formación y mantenimiento de las uniones estrechas |
Tabla 1. Resumen de los efectos de las principales micotoxinas sobre la integridad de la barrera intestinal.
Este conjunto de agresiones converge en el fenómeno del «intestino permeable» (Figura 1). La rotura de esta barrera permite la translocación masiva de antígenos luminales y bacterias hacia la circulación sistémica, un proceso que no solo debilita el estado de salud, sino que desencadena respuestas inflamatorias crónicas con un elevado coste metabólico para el animal (Gasperini et al., 2025; Smith et al., 2012).
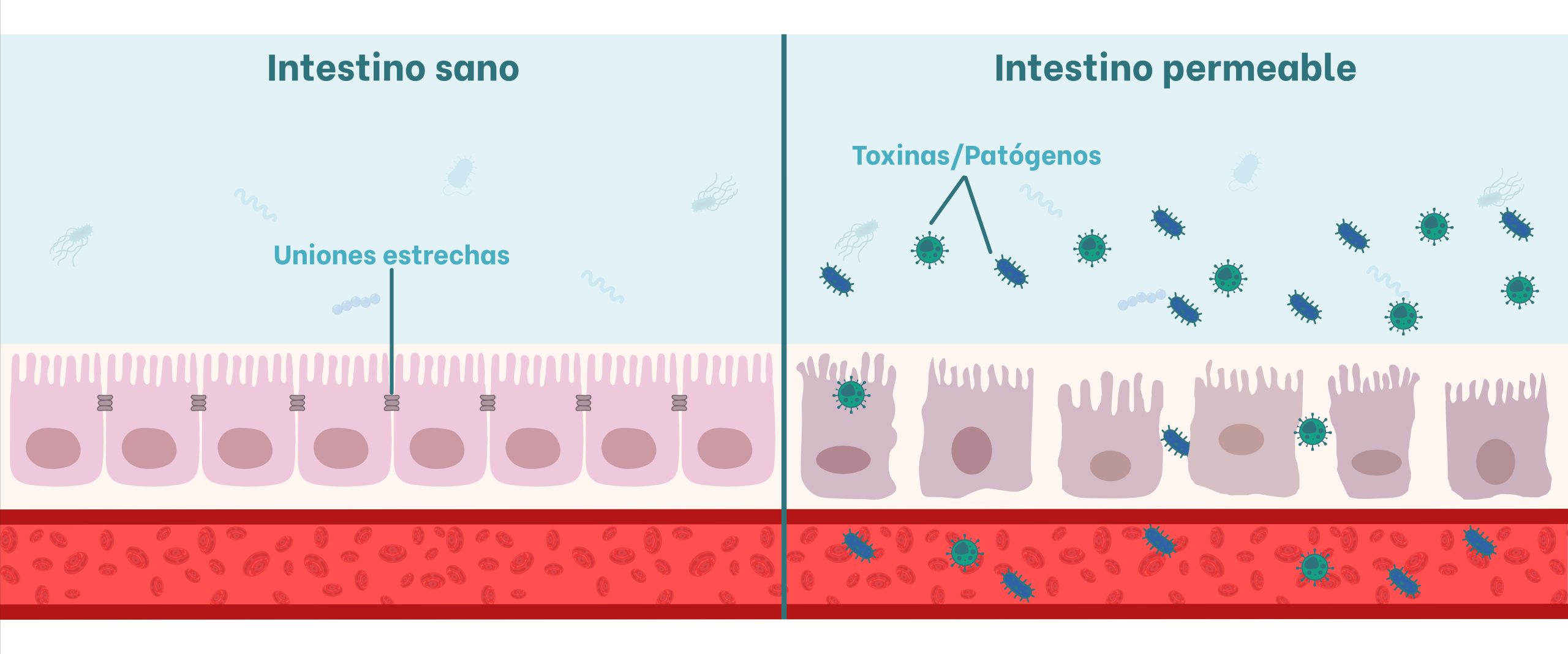
Figura 1. Representación del impacto de las micotoxinas en la barrera intestinal. A la izquierda, un epitelio sano con uniones estrechas funcionales; a la derecha, el fenómeno de «intestino permeable», donde la degradación de proteínas transmembrana y/o de andamiaje citoplasmático permite la translocación de toxinas y patógenos hacia el torrente circulatorio.
Microbiota: eje estratégico de la homeostasis
Más allá de ser una población residente, la microbiota intestinal debe considerarse un «órgano metabólico» dinámico que mantiene un equilibrio simbiótico con el hospedador (Alassane-Kpembi et al., 2019). La microbiota es fundamental para regular la integridad de la mucosa intestinal, así como para asegurar una correcta función inmunitaria y para garantiza una óptima absorción y el correcto metabolismo de los nutrientes (An et al., 2025; Celi et al., 2017).
Sus funciones se pueden clasificar en tres pilares: protectoras, estructurales y metabólicas.
En primer lugar, la microbiota desempeña funciones protectoras mediante el establecimiento de una barrera biológica competitiva. Este mecanismo impide la colonización de patógenos a través del desplazamiento de microorganismos invasores, de la competencia por sitios de recepción y de la producción activa de factores antimicrobianos (Celi et al., 2017; Guerre, 2020).
Por otro lado, sus funciones estructurales son vitales para la fortificación de la barrera gastrointestinal, induciendo la síntesis de inmunoglobulina A (IgA) y favoreciendo el sellado apical de las uniones estrechas (Celi et al., 2017).
Finalmente, atendiendo a las funciones metabólicas de la microbiota, esta permite la fermentación de residuos dietéticos no digeribles para producir ácidos grasos de cadena corta (SCFAs). Estos metabolitos no solo representan una fuente de energía celular primaria para el epitelio, sino que son pilares de la salud del colon y la síntesis de vitaminas esenciales, enzimas y aminoácidos (Celi et al., 2017; Zheng et al., 2018). Dentro de las funciones metabólicas también hay que destacar la de defensa, la microbiota es capaz de hidrolizar o reducir toxinas en metabolitos significativamente menos tóxicos antes de su absorción sistémica (Guerre, 2020; Shanmugasundaram et al., 2023). Esta capacidad de biotransformación, sumada a su participación en la comunicación a través del eje microbiota-intestino-cerebro, posiciona al ecosistema microbiano como el guardián de la homeostasis sistémica del animal (Celi et al., 2017; Guerre, 2020).
Micotoxinas: el desequilibrio del ecosistema microbiano
Las micotoxinas actúan como potentes agentes disruptores del equilibrio de la microbiota (Figura 2), induciendo estados de disbiosis mediante propiedades antimicrobianas directas o, de forma indirecta, a través de la toxicidad celular y la liberación de péptidos antimicrobianos que alteran el nicho ecológico intestinal (Guerre, 2020; Gasperini et al., 2025).
La exposición a la AFB1 conlleva una reducción de la diversidad filogenética, alterando la relación entre los principales filos y favoreciendo una dominancia de Firmicutes frente a Actinobacteria (Gasperini et al., 2025; Guerre, 2020). Por su parte, el DON ejerce una presión selectiva que modifica la abundancia taxonómica, este proceso reduce poblaciones de Proteobacteria mientras favorece el crecimiento de bacterias proinflamatorias como las Enterobacteriaceae, aumentando el desafío sanitario (Shanmugasundaram et al., 2023; Gasperini et al., 2025).
De manera similar, la ZEA impacta negativamente en la diversidad global, observándose una disminución crítica de bacterias beneficiosas en segmentos clave como el ciego y el colon en conejos, cerdos y ratones (Guerre, 2020; Gasperini et al., 2025). En el caso de la OTA, su presencia incrementa la abundancia relativa del género Bacteroides, vinculado a inflamación sistémica en proporciones elevadas, y reduce drásticamente las poblaciones productoras de ácido butírico, comprometiendo el principal sustrato energético de los colonocitos (Zhai et al., 2021). Finalmente, las fumonisinas (FB1 y FB2) interfieren en la sucesión natural de especies bacterianas, promoviendo la proliferación de géneros que comprometen la estabilidad del tracto gastrointestinal desde etapas tempranas (Guerre, 2020; Alassane-Kpembi et al., 2019).
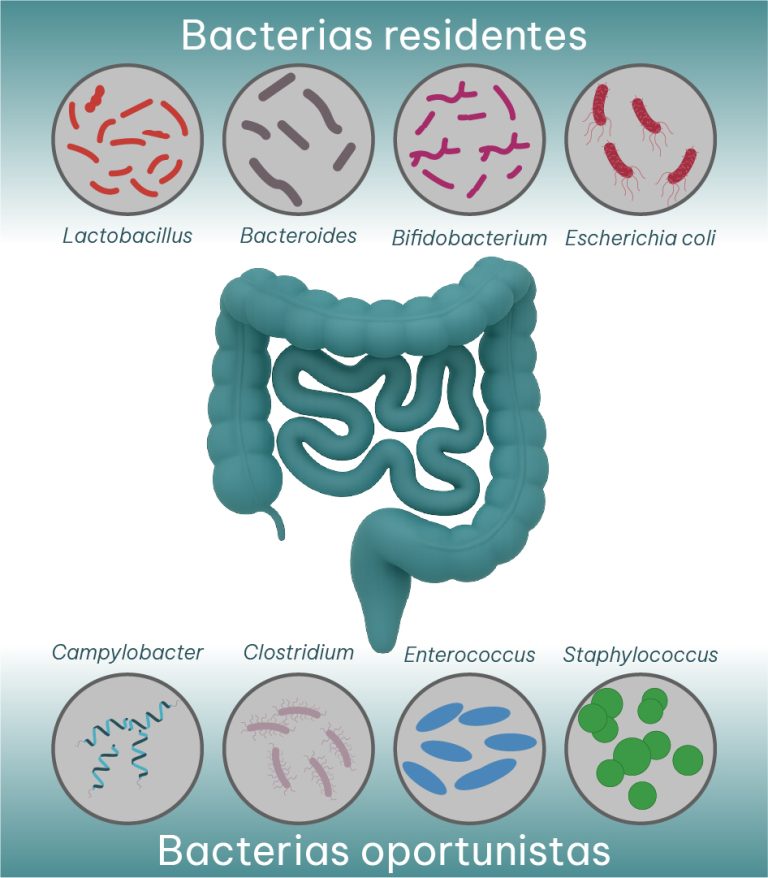
Figura 2. La composición de la microbiota está en equilibrio entre géneros bacterianos residentes (ej. Lactobacillus) y oportunistas o potencialmente patógenos (ej. Clostridium). Las micotoxinas causan un desequilibrio al disminuir las poblaciones de bacterias beneficiosas y aumentando las de bacterias patógenas.
Consecuencias clínicas y productivas
Todas las alteraciones descritas producidas por las diferentes micotoxinas a nivel intestinal, que pueden implicar la alteración de la integridad epitelial y la disbiosis de la población bacteriana, repercuten directamente en la salud de los animales, y con ello en su rendimiento productivo.
El fenómeno del intestino permeable facilita la translocación bacteriana de patógenos sistémicos como Salmonella Typhimurium y Escherichia coli. Estos microorganismos logran franquear la barrera intestinal para colonizar nódulos linfáticos mesentéricos y órganos vitales como el bazo, el hígado y los pulmones, provocando una respuesta inflamatoria sistémica crónica y la supresión de la respuesta inmunitaria específica (Guerre, 2020; Pierron et al., 2016).
Asimismo, un aumento en la translocación bacteriana de patógenos aumenta la predisposición de los animales a infecciones entéricas secundarias. En pollos de engorde, micotoxinas como el DON y la FB1 actúan como factores predeterminantes en la patogénesis de la enteritis necrótica por Clostridium perfringens (Antonissen et al., 2014; Shanmugasundaram et al., 2023; Guerre, 2020).
Por otro lado, la toxina T-2 representa una amenaza específica al inducir una disbiosis ileal profunda que eleva los niveles de lipopolisacáridos (LPS) en suero. Este evento activa cascadas inflamatorias hepáticas en cerdos, promoviendo patologías como la esteatosis y la infiltración celular, lo que compromete el metabolismo basal del animal (An et al., 2025; He et al., 2024).
Por su parte, el DON ejerce un efecto inhibitorio sobre transportadores críticos como el SGLT-1, responsable del transporte de glucosa y sodio. Esta interferencia no solo provoca una malabsorción de azúcares, sino que desencadena cuadros de diarrea crónica al comprometer la reabsorción de agua (Pierron et al., 2016; Smith et al., 2012).
Esta cascada de eventos impacta de forma determinante en los parámetros de rendimiento. La coexposición, incluso a dosis subclínicas, de fumonisinas y DON, reduce significativamente la ganancia de peso corporal y eleva de manera ineficiente el índice de conversión alimenticia (Shanmugasundaram et al., 2023; Pierron et al., 2016).
Finalmente, el cuadro se agrava por la inducción de anorexia y el rechazo del alimento. Esto es debido a que micotoxinas como el DON y la toxina T-2 estimulan de forma anómala las hormonas de la saciedad y diversas citoquinas que alteran la comunicación en el eje microbiota-intestino-cerebro. Este desequilibrio neuroendocrino limita drásticamente la ingesta energética, consolidando un retraso en el crecimiento que compromete la viabilidad económica de la explotación (Guerre, 2020; Smith et al., 2012; An et al., 2025).
Desde una perspectiva estrictamente productiva, el daño intestinal inducido por micotoxinas se traduce en una disminución directa de la rentabilidad de la explotación. El impacto comienza con un deterioro severo de la función de absorción nutricional; la exposición a estos metabolitos causa alteraciones histomorfológicas que incluyen el desprendimiento y la atrofia de las vellosidades, reduciendo drásticamente la superficie útil para la captación de nutrientes (Zhai et al., 2021; Pierron et al., 2016).
Conclusión
En conclusión, el control de la salud digestiva, mediante el mantenimiento de la integridad y permeabilidad intestinal, junto con la prevención de la disbiosis, constituye uno de los ejes centrales en la mitigación de la toxicidad inducida por micotoxinas. En este contexto, una comprensión profunda de los mecanismos mediante los cuales estas toxinas interactúan con el tracto gastrointestinal resulta esencial para el diseño de estrategias nutricionales eficaces, capaces de preservar la salud intestinal, minimizar el impacto fisiopatológico de las micotoxinas y, en consecuencia, optimizar el rendimiento productivo.


