Введение
Наряду с домашней птицей и крупным рогатым скотом, свиньи являются одним из самых восприимчивых видов животных к токсичности афлатоксинов. Среди различных разновидностей микотоксинов эта группа считается одной из самых токсичных и известна своей высокой распространенностью во всем мире и канцерогенным действием. В настоящее время известно более 20 различных типов афлатоксинов, среди которых следует выделить афлатоксин B1 (AFB1), признанный за его вредное воздействие как на людей, так и на животных (Popescu et al., 2022).
Афлатоксины могут вызывать серьезные проблемы у свиней, как при остром, так и при хроническом воздействии. Эти вещества оказывают токсическое воздействие в основном на печень, вызывая значительные нарушения в ее физиологии и функционировании (Pang et al., 2020). Длительное воздействие приводит к состояниям иммуносупрессии, которые связаны с увеличением смертности, ухудшением показателей продуктивности и снижением репродуктивной способности (Popescu et al., 2022). Более того, их токсичность напрямую связана с повышенной восприимчивостью к респираторным патогенам и, как следствие, с более высокой заболеваемостью респираторным синдромом свиней (Pang et al., 2020). AFB1 также связан с токсическим воздействием на желудочно-кишечный тракт, нервную систему, иммунные клетки и репродуктивные органы (Li et al., 2022).
С другой стороны, сообщалось, что токсичность, вызываемая афлатоксинами, в основном связана с их метаболитами. В частности, свиньи обладают меньшей способностью к детоксикации, чем другие виды животных, поскольку их способность к экскреции этих метаболитов ограничена, что повышает риск интоксикации и афлатоксикоза (Popescu et al., 2022). Эта детоксикация включает в себя ряд метаболических процессов, которые изучаются в рамках токсикокинетики. Токсикокинетика микотоксинов охватывает этапы от абсорбции этих загрязняющих веществ до их распределения в организме, метаболизма и, наконец, их экскреции. Эти процессы называются процессами ADME, и их изучение имеет фундаментальное значение для понимания токсичности микотоксинов и того, как она варьируется у разных видов животных (Schrenk et al., 2020).
Еще одним важным аспектом, связанным с токсикокинетикой AFB1 у свиней, является то, что некоторые метаболиты этого микотоксина были обнаружены у поросят, что указывает на возможность их передачи через плаценту во время беременности (Schrenk et al., 2020). Аналогичным образом, его попадание в молоко сделало процесс лактации возможным источником воздействия для новорожденных. Помимо этого, данный микотоксин был обнаружен в других продуктах питания для людей, таких как мясо и яйца. Поэтому воздействие кормов, загрязненных афлатоксинами, представляет риск не только для животных, но и для конечного потребителя, являясь проблемой пищевой безопасности (Li et al., 2022).
BIŌNTE® QUIMITŌX® PLUS: Токсикокинетическое исследование AFB1 на свиньях
Известно, что снижение пероральной биодоступности, определяемой как доля вещества, которая может попасть в кровь в активной форме, представляет собой безопасную и эффективную стратегию контроля токсичности микотоксинов. Путем контроля микотоксинов в момент абсорбции снижается их системное распределение и распределение их метаболитов, что уменьшает токсичность, которую они могут вызывать в различных органах, и их негативное влияние на здоровье и продуктивность животных.
В данном случае, посредством проведения токсикокинетического исследования in vivo, выполненного в сотрудничестве с Гентским университетом, были оценены эффекты BIŌNTE® QUIMITŌX® PLUS на пероральную биодоступность AFB1 у свиней, с регистрацией профиля плазменной концентрации AFB1 в зависимости от времени.
BIŌNTE® QUIMITŌX® PLUS — это антимикотоксиновое решение, сочетающее в себе минеральные ингредиенты для селективной и эффективной адсорбции этих токсинов, а также содержащее специфическую комбинацию натуральных экстрактов и отобранных дрожжей, обеспечивающих биопротекторный и постбиотический эффект. Таким образом, он представляет собой вариант широкого спектра действия с различными механизмами работы, эффективный в борьбе с негативным воздействием этих загрязняющих веществ на различные виды наземных животных.
Методология, использованная в данном исследовании, включала 8 самок поросят породы Бельгийский Ландрас х Пьетрен в возрасте 7 недель. Они были разделены на две экспериментальные группы, и после осле недельного периода адаптации был установлен перекрестный дизайн исследования (Рисунок 1).
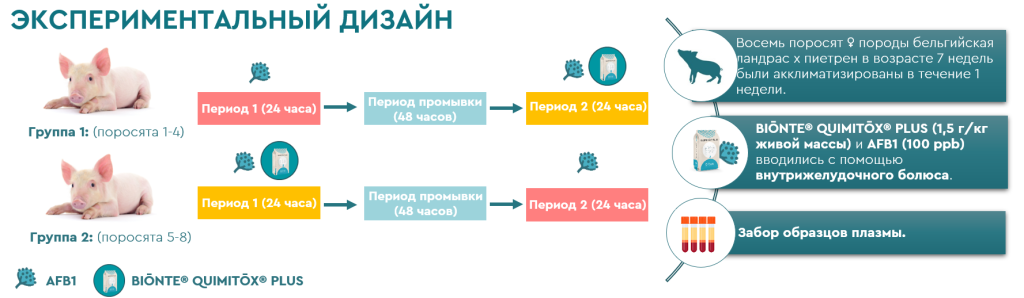
Рисунок 1. Экспериментальная схема.
Группа 1 в течение первого периода получала внутрижелудочный болюс AFB1 (100 ppb), после чего последовал период вымывания продолжительностью 48 часов, и, наконец, в течение второго периода она получила еще один болюс AFB1 (100 ppb) в сочетании с препаратом BIŌNTE® QUIMITŌX® PLUS в дозе 1,5 г/кг живой массы. С другой стороны, группа 2 в течение первого периода получала болюс AFB1 (100 ppb) вместе с препаратом BIŌNTE® QUIMITŌX® PLUS в той же дозировке, после чего последовала фаза вымывания, а во втором периоде она снова получила болюс AFB1 (100 ppb).
Контроль в ходе исследования заключался в отборе проб крови как до введения препаратов, так и через контролируемые интервалы времени после введения.
Токсикокинетический анализ включал изучение нескольких параметров, таких как площадь под кривой концентрации в плазме в зависимости от времени от 0 до 12 часов (AUC0→12), а также максимальная концентрация в плазме (Cmáx).
Эффект BIŌNTE® QUIMITŌX® PLUS на пероральное всасывание AFB1 оценивался путем сравнения токсикокинетических параметров на основе плазменных концентраций AFB1 в образцах, обработанных исключительно AFB1, по сравнению с показателями животных, подвергшихся воздействию AFB1 вместе с антимикотоксиновым препаратом.
Результаты испытаний: Эффективность BIŌNTE® QUIMITŌX® PLUS
Системное воздействие AFB1 было значительно ниже у тех поросят, которые получали AFB1 вместе с BIŌNTE® QUIMITŌX® PLUS (отмечено желтым цветом), по сравнению с теми, кто получал только AFB1 (отмечено красным цветом) (Рисунок 2). В частности, показатели AUC0→12 и Cmáx продемонстрировали снижение на 95% и 96% соответственно благодаря применению антимикотоксинового решения (Таблица 1).
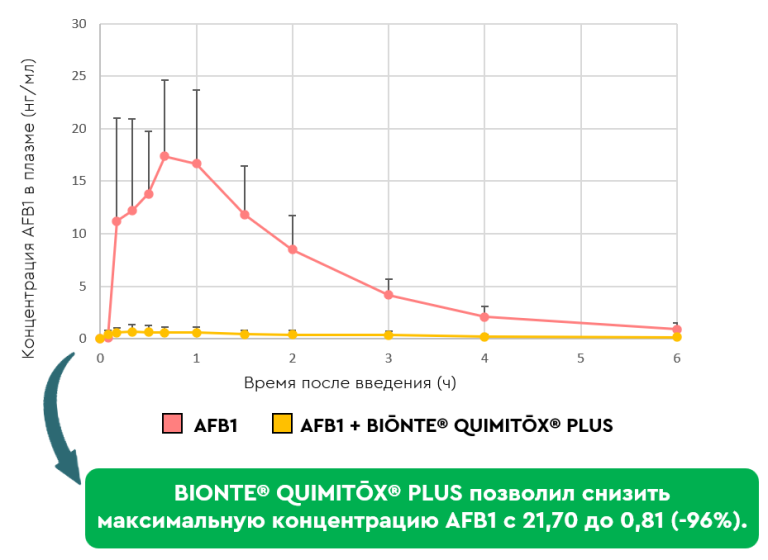
Рисунок 2. Профиль концентрации AFB1 в плазме крови в зависимости от времени после перорального приема дозы AFB1 (100 ppb) отдельно или в сочетании с BIŌNTE® QUIMITOX® PLUS.

Таблица 1. Основные токсикокинетические параметры AFB1 после перорального введения AFB1, отдельно или в сочетании с BIŌNTE® QUIMITŌX® PLUS (BQP).
Помимо подтверждения эффективности за счет снижения присутствия AFB1 в крови, результаты указали на быстрое действие BIŌNTE® QUIMITŌX® PLUS, что позиционирует его как основополагающую стратегию в борьбе с микотоксинами. Эти токсичные вещества быстро попадают в кровь после воздействия на животных, и именно поэтому эффективность и скорость действия должны идти рука об руку при разработке эффективных стратегий.
Заключение
Подводя итог,BIŌNTE® QUIMITŌX® PLUS продемонстрировал высокую эффективность в этом исследовании токсикокинетики in vivo, быстро и эффективно снижая общую системную подверженность свиней одному из наиболее известных токсичных микотоксинов, афлатоксину B1.


